Latihan 3.Buatlah 4 soal pilihan ganda dari kelompok anda
Contoh soal 1
Hitunglah volume pelarut yang harus ditambahkan jika 100 mL larutan KOH 0,1 M diencerkan sehingga konsentrasinya menjadi 0,01 M ?
a.100 mL
b1200mL
c.1000mL
d.1300mL
e.2000mL
Jawaban: c.1000mL
Pembahasan:
V1 = 100 mL
M1 = 0,1 M
M2 = 0,01 M
V1 . M1 = V2 . M2
100 . 0,1 = V2 . 0,01
10 = 0,01V2
V2 = 100,01
= 1000 mL
Jadi volume pelarut yang harus ditambahkan adalah 1000 mL
Contoh Soal 2
Berapa konsentrasi dari larutan asam asetat CH3COOH jika diketahui untuk titrasi 25 mL larutan CH3COOH tersebut diperlukan 15 mL larutan NaOH 0,05 M agar mencapai titik ekivalen?
a.0,03 M
b 3 M
c.0,06 M
d 0,6 M
e 0,3 M
Jawaban : a.0,03 M
Persamaan reaksi netralisasi CH3COOH dengan NaOH:
CH3COOH(aq) + NaOH(aq) → CH3COONa(aq) + H2O(l)
Dari persamaan reaksi, diperoleh: 1 mol CH3COOH 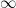 1 mol NaOH
1 mol NaOH
sehingga bisa dapat:
Contoh Soal 3
Sebanyak 40 mL larutan asam sulfat 0,25 M dititrasi dengan suatu basa bervalensi satu, dan ternyata dibutuhkan 57 mL basa tersebut. Berapakah kemolaran basa yang digunakan tersebut?
a.0,45 M
b0,35 M
c.2 M
d.0,33 M
e.0,37 M
Jawab:
Reaksi netralisasi terjadi antara asam sulfat H2SO4 (asam kuat bervalensi dua) dengan suatu basa bervalensi satu
Contoh soal 4
Berikut data hasil titrasi larutan HCL dengan larutan NaOH 0,1 M
Berdasarkan data tersebut,konsentrasi larutan HCL adalah
a.0,070 M
b0,075 M
c.0,080 M
d 0,133 M
e.0,143 M
Jawaban : b.0.075 M



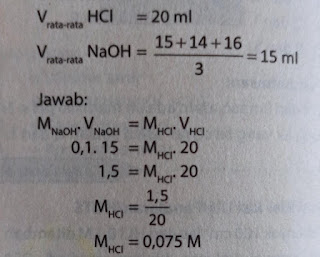



Tidak ada komentar:
Posting Komentar